지난 시간에는 주기율표의 역사들과 함께 20번 원소인 칼슘까지 적용되는 족과 주기의 경향성에 대해서 알아보았습니다.
혹시 지난번 내용들이 궁금하신 분들은 아래 링크를 이용해 주세요.
2021/01/04 - [화학을 배웁니다/화학 이론] - 주기율표 1 (소개 및 역사)
주기율표 1 (소개 및 역사)
오늘은 주기율표를 소개해드리면서 주기율표에 숨겨진 역사에 대해서 알아보는 시간을 갖도록 하겠습니다. 주기율표는 보통 중학교 과학시간에 처음 접하게 됩니다. 중학교 수준의 과학에서는
chemistry-station.tistory.com
2021/01/20 - [화학을 배웁니다/화학 이론] - 주기율표 2 (족과 주기)
주기율표 2 (족과 주기)
지난시간에는 주기율표를 소개해 드리면서 역사에 대해서 알아보는 시간을 가졌습니다. 혹시 지난번 내용이 궁금하신 분들이 아래 링크를 이용해주세요. 2021/01/04 - [화학을 배웁니다/화학 이론]
chemistry-station.tistory.com
이번 시간에는 20번 이후의 원소들에 적용될 수 있는 경향성들을 알아보도록 하겠습니다.
간략하게 복습을 해보면 주기율표의 세로줄을 족, 영어로는 family 라고 부르고 가로줄을 주기, 영어로 period라고 부릅니다.
그리고 20번 원소까지는 족이 하나씩 증가할 수록 최외각 전자의 수가 한개씩 증가하며
주기가 하나씩 증가할 수록 전자껍질의 수가 증가하는 경향성을 가집니다.
또한 수소부터 칼슘까지의 원소들은 s 오비탈과 p 오비탈로만 구성되어 있고 이 오비탈에 전자가 차례대로 채워집니다. 전자가 채워진 방식은 다음의 표를 확인 해 주세요.
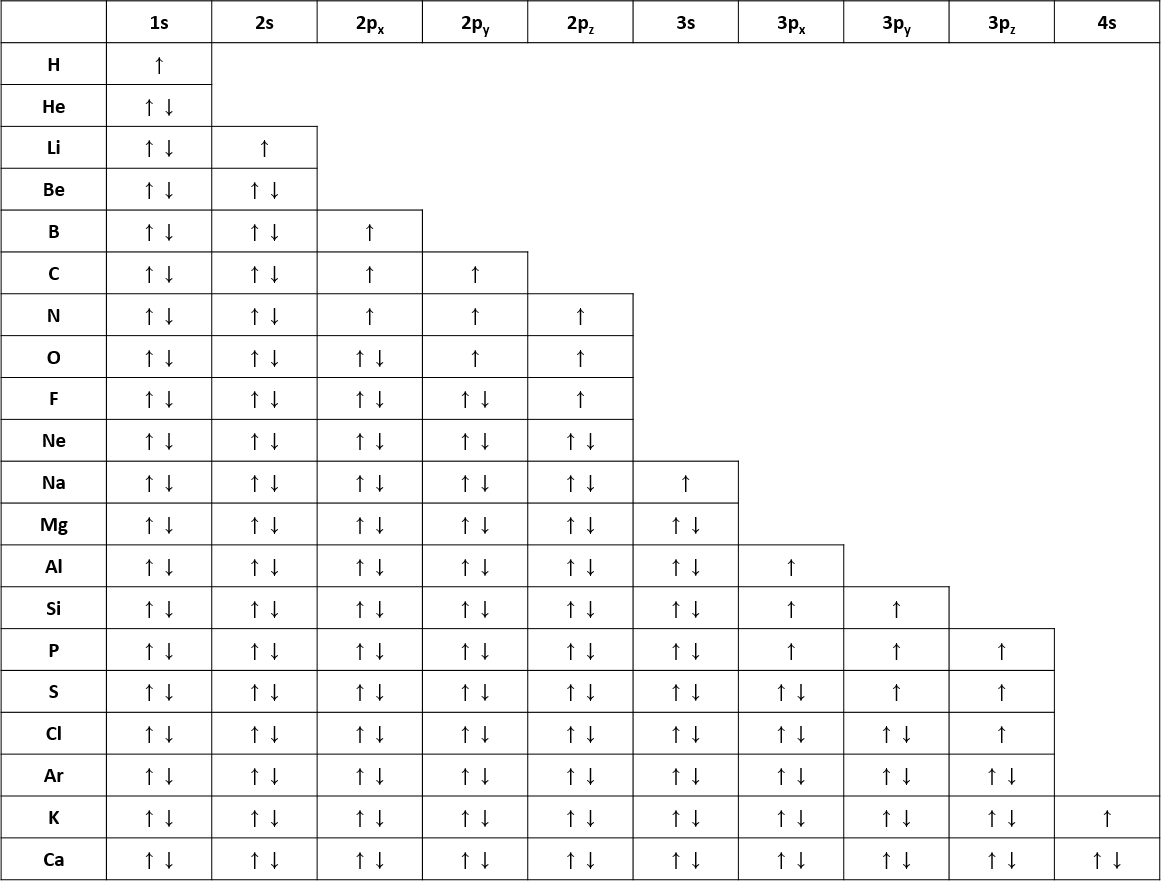
전자가 1s → 2s → 2p → 3s → 3p → 4s 의 순서대로 차례대로 채워지는 것을 보실 수 있습니다.
s 오비탈에 먼저 전자가 채워지고 그다음에 p 오비탈에 전자가 채워지는 경향성이 보이실 겁니다.
여기서 잠깐!!
자꾸 오비탈이라는 말이 나와서 어렵게 느껴지실 수 있는데
쉽게 설명하면 오비탈은 전자가 들어갈 수 있는 집이라고 생각하시면 됩니다.
그리고 그 집들의 이름이 s, p, d, 또는 f 인 것입니다.
한가지 더 추가로 알려드리면
s 집에는 방이 1개, p 집에는 방이 3개, d 집에는 방이 5개, f 집에는 방이 7개 있으며
그 방의 이름들은 아래에 나와있는 그림에서 살펴 보실 수 있습니다.
가령 p 집에 있는 방들의 이름은 각각 x, y, z 가 되는 것입니다.
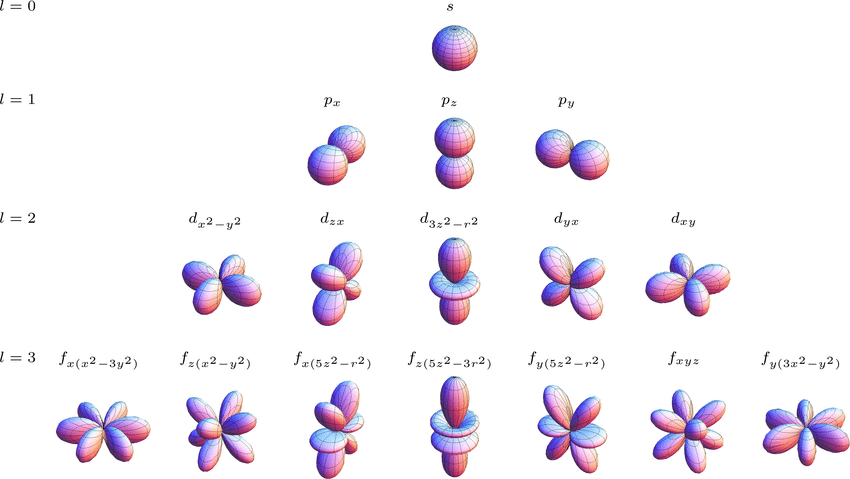
자, 그런데 지난시간에 예고한 바와 같이 21번 원소인 스칸듐부터 예외사항이 생겨버립니다.
바로 d 오비탈이라는 새로운 친구가 등장하게 되면서 전자가 s 오비탈, p 오비탈의 순서로 채워지지 않게 됩니다.
이렇게 추가된 경향성을 모두 설명할 수 있는 원리가 바로 쌓음 원리, Aufbau principle이라고 합니다. 이 원리에 의하면 4s 오비탈 이후에 4p 오비탈에 전자가 채워지는 것이 아닌 3d 오비탈에 채워지게 됩니다.
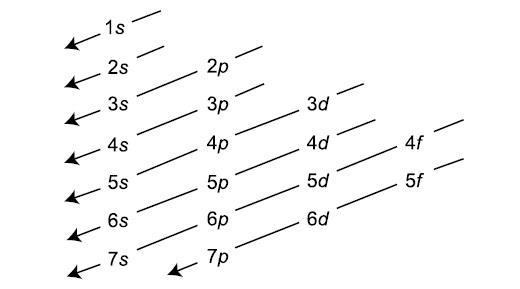
이 재미있는 원리는 다음 그림을 한번씩 그려보시면 금방 이해하실 수 있습니다.
먼저 1s 부터 7p 까지 한줄씩 쓰신다음 오른쪽 위에서 왼쪽 아래 방향으로 대각선을 긋게 되면 전자가 채워지는 순서를 완성하실 수 있습니다. 추가로 이 Aufbau principle은 닐스 보어(Niels Bohr)와 볼프강 파울리(Wolfgang Pauli)에 의해서 만들어졌습니다.
이 쌓음원리에 의하여 21번 스칸듐부터는 전자가 차례로 쌓이게 됩니다.
그리고 이 쌓음원리는 앞서 배웠던 1번 수소부터 20번 칼슘까지의 전자배열을 모두 설명할 수 있게 됩니다.
하지만 이렇게 단순한 규칙으로 모든 화학의 원리가 설명될 리가 없지요!
다음 시간에는 이 쌓음원리의 예외 사항들을 한번 알아보도록 하겠습니다.
너무 어렵게 생각하지 않으셔도 됩니다. 화학 발전소와 함께 하나씩 차근 차근 알아보아요!
이상 화학 발전소였습니다.
질문은 댓글로!
유용하게 보셨다면 좋아요!
부탁드려요!
'화학을 배웁니다 > 화학 이론' 카테고리의 다른 글
| 주기율표 2 (족과 주기) (2) | 2021.01.20 |
|---|---|
| 주기율표 1 (소개 및 역사) (0) | 2021.01.04 |
| 화학 작용기 (Functional Groups) (0) | 2020.12.30 |
| 화학의 정의 (0) | 2020.11.23 |
| 탄소 화합물 (Compounds of Carbon) 1 (0) | 2020.11.19 |
